Echte Lösung ist eine homogene Mischung aus zwei oder mehr Stoffen, in der die im Lösungsmittel gelösten (gelösten) Stoffe eine Partikelgröße von weniger als 10-9 nm oder 1 nm aufweisen. Die einfache Lösung von Zucker in Wasser ist ein Beispiel für eine echte Lösung.
Die gelösten Partikel sind mit bloßem Auge und unter dem stärksten Mikroskop unsichtbar. Außerdem können echte Lösungspartikel sowohl Pergament als auch Filterpapier diffundieren oder passieren. Noch wichtiger ist, dass eine echte Lösung keinen Tyndall-Effekt (Streulicht) zeigt.
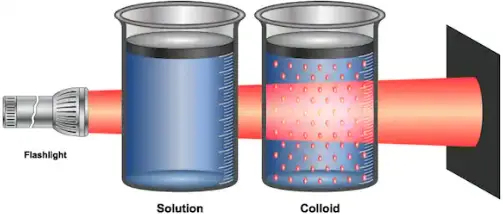
Eine kolloidale Lösung, auch als kolloidale Suspension bezeichnet, ist eine Lösung, in der ein Material gleichmäßig in einer Flüssigkeit suspendiert ist (Zwischenprodukt aus echter Lösung und Suspension). Rauch von einem Feuer ist ein Beispiel für ein kolloidales System, in dem winzige Feststoffpartikel in der Luft schweben. Die Partikelgröße in kolloidaler Lösung liegt im Bereich von 1 nm bis 100 nm und ist mit bloßem Auge nicht zu erkennen, ihre Streuung kann jedoch mit Hilfe eines Mikroskops beobachtet werden.
Kolloidale Lösung zeigt normalerweise Tyndall-Effekt (Streulicht). Auch Partikel in der kolloidalen Lösung zeigen Brownsche Bewegungen.
Eine Suspension ist eine heterogene Mischung, in der sich die gelösten Partikel nicht auflösen, sondern im Großteil des Lösungsmittels suspendiert werden und frei im Medium schweben. Wenn Schlamm in Wasser gelöst und kräftig gerührt wird, verteilen sich Schlammpartikel gleichmäßig im Wasser. Nach einiger Zeit setzen sich die Partikel dieser Lösung aufgrund des Einflusses der Schwerkraft unter Wasser ab. Dies ist ein gutes Beispiel für eine Aussetzung. Suspensionspartikel sind mit bloßem Auge sichtbar.
Die Größe der Partikel bei Suspension ist größer als 100 nm. Suspensionspartikel passieren Filterpapier und Pergamentpapier nicht. Außerdem kann eine Aufhängung einen Tyndall-Effekt (Streulicht) zeigen oder nicht.
Weiterlesen : Unterschied zwischen Kolloid und Suspension mit Beispielen
Wahre Lösung vs. Kolloidale Lösung vs. Aussetzung in Tabellenform
| VERGLEICHSGRUNDLAGE | WAHRE LÖSUNG | KOLLOIDALE LÖSUNG | SUSPENSION |
| Beschreibung | Echte Lösung ist eine homogene Mischung aus zwei oder mehr Stoffen, in der die im Lösungsmittel gelösten (gelösten) Stoffe eine Partikelgröße von weniger als 10-9 nm oder 1 nm aufweisen. | Eine kolloidale Lösung, auch kolloidale Suspension genannt, ist eine Lösung, in der ein Material gleichmäßig in einer Flüssigkeit suspendiert ist. | Eine Suspension ist eine heterogene Mischung, in der sich die gelösten Partikel nicht auflösen, sondern im Großteil des Lösungsmittels suspendiert werden und frei im Medium schweben. |
| Größe der Partikel | Die Teilchengrößen in einer echten Lösung sind Moleküle mit einem Durchmesser von weniger als 1 nm. | Die Partikelgröße in kolloidaler Lösung liegt im Bereich zwischen 1 nm bis 100 nm. | Die Größe der Partikel bei Suspension ist größer als 100 nm. |
| Tyndall-Effekt | Die wahre Lösung zeigt keinen Tyndall-Effekt (Streulicht). | Kolloidale Lösung zeigt normalerweise Tyndall-Effekt (Streulicht). | Die Aufhängung kann einen Tyndall-Effekt (Streulicht) zeigen oder nicht. |
| Sichtbarkeit / Aussehen von Partikeln | Die gelösten Partikel sind mit bloßem Auge und unter dem stärksten Mikroskop unsichtbar. | Die gelösten Partikel sind für das bloße Auge unsichtbar, ihre Streuung kann jedoch mit Hilfe eines Mikroskops beobachtet werden. | Die gelösten Partikel sind sogar mit bloßem Auge sichtbar oder können mit Hilfe eines Mikroskops gesehen werden. |
| Art der Lösung | Homogen. | Heterogen. | Heterogen. |
| Farbe der Lösung | Hängt von der Natur des löslichen Salzes oder der Ionen ab. | Hängt von der Größe der kolloidalen Partikel ab. | Abhängig von der Farbe der Schwebstoffe. |
| Brownsche Bewegungen | Teilchen in der wahren Lösung zeigen keine Brownschen Bewegungen. | Teilchen in der kolloidalen Lösung zeigen Brownsche Bewegungen. | Die Teilchen zeigen Brownsche Bewegungen. |
| Sedimentation | Partikel in echter Lösung unterliegen keiner Sedimentation. | Kolloide Partikel unterliegen keiner Sedimentation. | In Suspension unterliegen Partikel einer Sedimentation. |
| Filtrierbarkeit (Passage durch Pergament und Filterpapier). | Echte Lösungspartikel können sowohl Pergament als auch Filterpapier diffundieren oder passieren. | Kolloidpartikel können ein Filterpapier passieren, aber nicht Pergamentpapier. | Suspensionspartikel passieren Filterpapier und Pergamentpapier nicht. |
| Äußere Erscheinung | Transparent. | Durchscheinend. | Undurchsichtig. |
| Anzahl der Phasensysteme | Einphasensystem. | Zweiphasige Systeme. | Zweiphasensysteme. |
| Stabilität | Stabil | Stabil | Metastabil. |
| Beispiel | Zuckerlösung in Wasser. | Stärke in Wasser gelöst. | Erde in Wasser gelöst. |
Weiterlesen: Unterschied zwischen Sol und Gel mit Beispielen
