Erhalten Sie klare Einblicke in den Unterschied zwischen organischen und anorganischen Verbindungen. Vergleichsgrundlagen sind: Beschreibung, Dichte, Löslichkeit, Bildung, Leitfähigkeit, Siede- und Schmelzpunkte, Beispiele, Viskosität, Reaktivität und mehr.
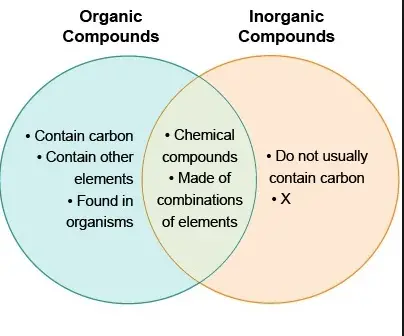
Hauptunterschiede
- Organische Verbindungen sind eine Klasse chemischer Verbindungen, in denen ein oder mehrere Kohlenstoffatome kovalent mit Atomen anderer Elemente verbunden sind, am häufigsten Wasserstoff, Sauerstoff oder Stickstoff. Andererseits ist eine anorganische Verbindung jede Verbindung, der ein Kohlenstoffatom fehlt.
- Die Dichte der Verbindung basiert normalerweise auf der Größe des Moleküls gegenüber der Größe der Atome im Molekül. Aufgrund des Vorhandenseins von mehr Wasserstoffatomen in organischen Verbindungen neigen organische Verbindungen dazu, typischerweise weniger dicht zu sein als anorganische Verbindungen. Dies liegt daran, dass Wasserstoff unter allen Atomen das Atom mit der niedrigsten Dichte ist.
- Anorganische Verbindungen sind in Wasser gut löslich. Dies liegt daran, dass sie ionische Bindungen zwischen Molekülen haben. Ionenbindungen dissoziieren im Wasser leicht in positive und negative Ionen. Andererseits haben die meisten organischen Verbindungen kovalente Bindungen zwischen Molekülen und sind daher in Wasser unlöslich, obwohl sie in anderen organischen Lösungsmitteln löslich sind.
- Organische Verbindungen werden als Ergebnis von Einwirkungen lebender Organismen gebildet, während anorganische Verbindungen aufgrund von natürlichen Prozessen ohne Bezug zu irgendeiner Lebensform oder als Ergebnis menschlicher Experimente im Labor gebildet werden.
- In den meisten wässrigen Lösungen sind organische Verbindungen typischerweise schlechte Strom- und Wärmeleiter. Anorganische Verbindungen in wässrigen Lösungen sind gute Stromleiter, denn sie haben eine hohe Ionisationsfähigkeit und das macht sie zu besseren Leitern.
- Anorganische Verbindungen sind Salz, Metalle, Silber, Schwefel, reiner Diamant, Stoffe aus einzelnen Elementen und Stoffe, die keinen an Wasserstoff gebundenen Kohlenstoff enthalten. Andererseits umfassen Beispiele für organische Verbindungen Nukleinsäuren, Saccharose, Enzyme, Benzol, Methan, Fette und Ethanol.
- Anorganische Verbindungen haben eine schnellere Gesamtreaktionsgeschwindigkeit als organische Verbindungen. Stabile organische Verbindungen sind im Allgemeinen aufgrund des Vorhandenseins von kovalenten Bindungen, die schwer zu brechen sind, nicht reaktiv. Andererseits haben anorganische Verbindungen ionische Bindungen, die leicht brechen; Dies macht sie sehr reaktiv und wird immer mit allem reagieren, was verfügbar ist.
- Die Viskosität jeder Verbindung hängt von intermolekularen Kräften zwischen Molekülen ab. Je stärker die intermolekularen Kräfte sind, desto höher ist die Viskosität. Die intermolekularen Kräfte organischer Verbindungen sind schwach, ihre Viskosität tendenziell niedrig. Anorganische Verbindungen hingegen neigen dazu, starke intermolekulare Kräfte aufzuweisen, wie beispielsweise Wasserstoffbrückenbindungen, daher haben sie eine höhere Viskosität.
- Organische Verbindungen haben einen relativ hohen Schmelz- und Siedepunkt im Vergleich zu anorganischen Verbindungen, die im Allgemeinen einen niedrigen Schmelz- und Siedepunkt haben.
- Organische Verbindungen sind biologischer und komplexer Natur im Vergleich zu anorganischen Verbindungen, die einfacher und mineralischer Natur sind.
- Anorganische Verbindungen bilden leicht Salz, während organische Verbindungen kein Salz bilden können.
- Organische Verbindungen haben Kohlenstoffatome, die durch eine Kohlenwasserstoffbindung an Wasserstoffatome gebunden sind, während anorganische Verbindungen eine solche Bildung nicht aufweisen.
- Anorganische Metalle enthalten Metallatome, während organische Verbindungen dies nicht tun.
Lesen Sie auch : Unterschied zwischen organischer und anorganischer Chemie
Unterschied zwischen organischen und anorganischen Verbindungen in Tabellenform
| Vergleichspunkte | Organische Verbindung | Anorganische Verbindung |
| Definition | Organische Verbindungen sind eine Klasse chemischer Verbindungen, in denen ein oder mehrere Kohlenstoffatome kovalent mit Atomen anderer Elemente verbunden sind, am häufigsten Wasserstoff, Sauerstoff oder Stickstoff. | Eine anorganische Verbindung ist jede Verbindung, der ein Kohlenstoffatom fehlt. |
| Dichte | In der Regel weniger dicht. | Neigen Sie dazu, dichter zu sein. |
| Löslichkeit in Wasser | Sind in Wasser unlöslich. | Gut löslich in Wasser. |
| Formation | Organische Verbindungen werden durch die Wirkung lebender Organismen gebildet. | Anorganische Verbindungen werden aufgrund von natürlichen Prozessen ohne Bezug zu irgendeiner Lebensform oder als Ergebnis menschlicher Experimente im Labor gebildet. |
| Leitfähigkeit | In den meisten wässrigen Lösungen sind organische Verbindungen typischerweise schlechte Strom- und Wärmeleiter. | In den meisten wässrigen Lösungen sind anorganische Verbindungen typischerweise gute Strom- und Wärmeleiter |
| Beispiele | Beispiele für organische Verbindungen umfassen Nukleinsäuren, Saccharose, Enzyme, Benzol, Methan, Fette und Ethanol. | Anorganische Verbindungen sind Salz, Metalle, Silber, Schwefel, reiner Diamant, Stoffe aus einzelnen Elementen und Stoffe, die keinen an Wasserstoff gebundenen Kohlenstoff enthalten. |
| Reaktivität | Stabile organische Verbindungen sind nicht reaktiv. | Anorganische Verbindungen haben eine schnellere Gesamtreaktionsgeschwindigkeit. |
| Viskosität | Die intermolekularen Kräfte organischer Verbindungen sind schwach, ihre Viskosität tendenziell niedrig. | Anorganische Verbindungen hingegen neigen dazu, starke intermolekulare Kräfte aufzuweisen, wie beispielsweise Wasserstoffbrückenbindungen, daher haben sie eine höhere Viskosität. |
| Schmelz- und Siedepunkt | Organische Verbindungen haben einen relativ hohen Schmelz- und Siedepunkt. | Anorganische Verbindungen, die im Allgemeinen einen niedrigen Schmelz- und Siedepunkt haben. |
| Wesen der Existenz | Organische Verbindungen sind biologischer und komplexer Natur | Anorganische Verbindungen sind einfach und mineralisch. |
| Salzbildung | Sie bilden kein Salz. | Sie bilden oder machen leicht Salz. |
| Existenzform | Haben Kohlenstoffatome, die durch eine Kohlenwasserstoffbindung an Wasserstoffatome gebunden sind. | Haben Sie keine solche Bildung. |
| Komponenten | Sie enthalten keine Metallatome. | Metallatome enthalten. |
Ähnlichkeiten zwischen organischen und anorganischen Verbindungen
- Beide können in ihrer Struktur Kohlenstoffatome enthalten.
- Beide können in organischen Lösungsmitteln löslich sein.
- Beide haben intermolekulare Bindungen.
Zusammenfassung
Lesen Sie auch: Unterschied zwischen organischen und anorganischen Polymeren
Organische Verbindungen sind eine Klasse chemischer Verbindungen, in denen ein oder mehrere Kohlenstoffatome kovalent mit Atomen anderer Elemente verbunden sind, am häufigsten Wasserstoff, Sauerstoff oder Stickstoff. Andererseits ist eine anorganische Verbindung jede Verbindung, der ein Kohlenstoffatom fehlt.